Do pobierania, preparatyki i przechowywania krwi i jej składników należy używać wyłącznie zestawów pojemników i pojemników plastikowych dopuszczonych do obrotu w dopuszczonych do obrotu w Polsce i posiadających odpowiednie świadectwa rejestracji.
Płyny konserwujące
W przypadku procedur pobierania krwi i składników krwi metodami manualnymi i aferezy zaleca się stosowanie komercyjnych płynów konserwujących zgodnych z Farmakopeą Europejską i posiadających znak CE.
Pojemnik macierzysty, do którego pobierana jest krew, zawiera 63-70 ml płynu konserwującego. Płyn ten zapobiega krzepnięciu krwi i zawiera składniki odżywcze, umożliwiając przechowywanie krwi i jej składników. Płyn konserwujący powinien być sterylny i apirogenny.
Roztwór CPDA-1
Umożliwia przechowywanie krwi pełnej lub koncentratu krwinek czerwonych (RBC) w temperaturze od 2°C do 6°C przez 35 dni.
Roztwór CPD
Roztwór CPD umożliwia przechowywanie krwi pełnej lub koncentratu krwinek czerwonych w temperaturze od 2°C do 6°C przez okres do 21 dni. Najczęściej roztwór ten znajduje się w pojemniku macierzystym zestawów, które zawierają również pojemnik z roztworem wzbogacającym.
Roztwór ACD-A
Zaleca się stosowanie zestawów pojemników z tym roztworem wyłącznie do ręcznych procedur plazmaferezy. Roztwór ACD jest również powszechnie stosowany jako antykoagulant podczas zautomatyzowanych procedur plazmaferezy i cytaferezy (czasami 4% roztwór cytrynianu sodu jest zalecany jako antykoagulant do zautomatyzowanych procedur plazmaferezy).
Roztwory wzbogacające (uzupełniające)
Większość roztworów uzupełniających (ADSOL, AS-2, SAGM) zawiera chlorek sodu, adeninę, glukozę i mannitol. Inne zawierają cytrynian trisodowy, mannitol, diwodorofosforan sodu lub guanozynę.
Wspierają one żywotność czerwonych krwinek zawartych w koncentratach uzyskanych po usunięciu osocza. Objętość dodawanych roztworów waha się od 80 do 110ml. Zastosowanie roztworów wzbogacających umożliwia przechowywanie krwinek czerwonych w temperaturze od 2°C do 6°C przez okres do 42 dni.
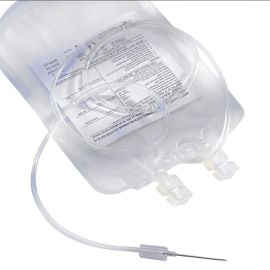
Zasady przygotowania w plastikowych pojemnikach
Integralnie połączone pojemniki tworzą zamknięty system, który zapobiega skażeniu bakteryjnego krwi podczas preparatyki.
Aby odblokować dreny łączące pojemniki, często konieczne jest zerwanie membrany u podstawy jednego z pojemników. Aby zapobiec mieszaniu się zawartości poszczególnych pojemników, należy użyć plastikowych zacisków lub kleszczy hemostatycznych przyłożonych do drenów.
Aby oddzielić od siebie poszczególne pojemniki, należy przeciąć łączący je dren, po zamknięciu go spawarką dielektryczną lub metalowymi zaciskami.
Zamknięcie drenu metalowym zaciskiem jest tylko tymczasowe i musi zostać wymienione przed zakończeniem preparacji należy zastąpić trwałym i szczelnym uszczelnieniem wykonanym przy użyciu spawarki. Każda spoina musi być sprawdzona wzrokowo, oceniając jej szczelność.
Przed pobraniem krwi pełnej należy zdecydować, jakiemu preparatowi zostanie ona poddana i w zależności od tego wybrać odpowiedni zestaw pojemników. Rozdzielenie krwi na jej składniki można przeprowadzić zarówno przy użyciu ręcznych, jak i automatycznych pras ekstrakcyjnych.
Przechowywanie krwi i jej składników w plastikowych pojemnikach
Pojemniki do pobierania krwi i pojemniki satelitarne wchodzące w skład zestawu są wykonane z polichlorku winylu (PVC). Tworzywo to (nieoznaczone żadnym symbolem ani oznaczeniem PL 146) działa stabilizująco na błonę komórkową erytrocytów i chroni czerwone krwinki przed hemolizą podczas przechowywania w stanie ciekłym. Jest stabilny do -90°C i pozwala na przechowywanie osocza w stanie zamrożonym, krioprecypitat i KKP.
Do przechowywania komórkowych składników krwi lub komórek macierzystych w stanie zamrożenia w temperaturze poniżej -90°C, wyłącznie pojemniki kriogeniczne wykonane z poliolefiny lub teflonu. Po odpowiednim przygotowaniu składnika należy go przenieść do pojemnika kriogenicznego.
Wlot pojemnika kriogenicznego powinien być natychmiast zamknięty przy użyciu specjalnego uszczelniacza. Niedopuszczalne jest używanie do zamrażania metalowych pojemników.
Przechowywanie i data ważności
1. Krew pełną przeznaczoną do transfuzji należy jak najszybciej po pobraniu umieścić w temperaturze od 2°C do 6°C i przechowywać w tej temperaturze od 2°C do 6°C i przechowywać w tej temperaturze. Dopuszczalne jest przechowywanie krwi do 2 godzin po pobraniu w temperaturze pokojowej, aby nastąpiła fagocytozy bakterii, które mogłyby dostać się do pojemnika. Data ważności krwi pełnej pobranej do płynu CPD wynosi 21 dni, natomiast krwi pobranej do płynu CPDA-1: 35 dni.
2. Jeśli krew jest przeznaczona do dalszego przygotowania w celu uzyskania KKP, należy ją jak najszybciej schłodzić do temperatury od 20°C do 24°C i przechowywać w tej temperaturze nie dłużej niż 5 godzin do momentu rozpoczęcia preparatyki. Jeśli nie można rozpocząć preparatyki w tym czasie, krew pełną należy jak najszybciej schłodzić do temperatury od 2°C do 6°C i przechowywać w tej temperaturze do dalszego przygotowania, podczas którego nie uzyskuje się KKP jest uzyskiwany.
Wskazania do stosowania
Konserwowana krew pełna jest przede wszystkim materiałem do izolacji składników krwi, a wskazania do jej stosowania w krwiolecznictwie są bardzo ograniczone.
Powinna być stosowana tylko w tych przypadkach, w których występuje jednocześnie niedobór erytrocytów i znaczny spadek objętości krwi krążącej (> 25%), a także w celu przygotowania składników do transfuzji wymiennej noworodków.
Przeciwwskazania
1. niedokrwistość bez zmniejszenia objętości krwi,
2. różne rodzaje nietolerancji osocza,
3. nietolerancja spowodowana alloimmunizacją antygenami leukocytów.
Środki ostrożności podczas stosowania
1. zgodność serologiczna musi zostać potwierdzona przed transfuzją za pomocą odpowiednich laboratoryjnych (test zgodności),
2. należy przetaczać przez filtr zatrzymujący mikroagregaty.








Validate your login